Thủ Thuật về Thành phần phần trăm theo khối lượng của nguyên tố Fe trong hợp chất FeO là Cho Fe = 56 O = 16 Mới Nhất
Bùi Minh Chính đang tìm kiếm từ khóa Thành phần phần trăm theo khối lượng của nguyên tố Fe trong hợp chất FeO là Cho Fe = 56 O = 16 được Cập Nhật vào lúc : 2022-04-01 08:52:06 . Với phương châm chia sẻ Kinh Nghiệm Hướng dẫn trong nội dung bài viết một cách Chi Tiết 2022. Nếu sau khi đọc tài liệu vẫn ko hiểu thì hoàn toàn có thể lại Comment ở cuối bài để Tác giả lý giải và hướng dẫn lại nha.
Đề bài
Phần trắc nghiệm (3 điểm)
Câu 1. Nguyên tử X nặng 5,312.10-23 gam, đó là nguyên tử của nguyên tố hoá học nào sau đây?
A. O: 16 đvC
B. Fe: 56 đvC.
C. S: 32 đvC
D. P: 31 đvC.
Câu 2. Cho công thức hoá học sau Al2(SO4)3. Phân tử có tổng số nguyên tử là
A.15 nguyên tử.
B. 5 nguyên tử.
C. 17 nguyên tử.
D. 10 nguyên tử
Câu 3. Để tách rượu ra khỏi hỗn hợp rượu lẫn nước, dùng cách nào sau đây?
A. Lọc.
B. Dùng phễu chiết.
C. Chưng cất.
D. Đốt
Câu 4. Trong những công thức hoá học sau : O2, N2, Al, Al2O3, H2, AlCl3, H2O, P.
Số đơn chất là
A. 4. B. 3.
C. 5. D. 6.
Câu 5. Nguyên tử của nguyên tố A nặng hơn nguyên tử của nguyên tố B 9 lần, nguyên tử của nguyên tố B nhẹ bằng (3 over 10) nguyên tử của nguyên tố C, nguyên tử của nguyên tố C bằng một nửa nguyên tử brom. Vậy A, B, C là những nguyên tố nào sau đây?
A. Mg, N, C.
B. Ag, C, Ca.
C. Pb, Zn, Ca.
D. O, Fe, C.
Câu 6. Công thức hoá học của những oxit do sắt kẽm kim loại Fe(III), Pb(IV), Ca(II) lần lượt là
A. FeO, PbO2, CaO.
B. Fe2O3, PbO, CaO.
C. Fe2O3, PbO, Ca2O.
D. Fe2O3, PbO2, CaO.
Phần tự luận (7 điểm)
Nguyên tử của nguyên tố A có 12 proton, có 2 electron ở lớp ngoài cùng, nguyên tử này nặng bằng 3/2 nguyên tử oxi.
a) Vẽ sơ đồ cấu trúc nguyên tử của nguyên tố A.
b) Tính nguyên tử khối của A.
c) Hạt nhân nguyên tử A có bao nhiêu nơtron?
Lời giải rõ ràng
Phần trắc nghiệm (3 điếm)
Trả lời đúng mỗi câu được 0,5 điểm
Câu 1. C
Biết khối lượng nguyên tử (gam), tìm nguyên tử khối:
1 đvC có khối lượng là
(1,9923.10^ - 23dfrac112 = 0,166.10^ - 23(g))
Suy ra nguyên tử khối là:
(5,312.10^ - 23.dfrac10,166.10^ - 23 = 32(đvc).)
Câu 2. C
Trong 1 phân tử Al2(SO4)3 có chứa 2 nguyên tử Al, 3 nguyên tử S và 12 nguyên tử O
=> Tổng số nguyên tử có trong phân tử là: 2 + 3 + 12 = 17 nguyên tử
Câu 3. C
Do nhiệt độ sôi của nước và rượu rất khác nhau, nên để thu được rượu tinh khiết ta hoàn toàn có thể dùng giải pháp chưng cất
Câu 4. C
Đơn chất là những chất được tạo nên là 1 nguyên tố hóa học.
Những đơn chất là: O2, N2, Al, H2, P.
Câu 5. B
Để làm được thắc mắc này, ta cần ghi nhớ nguyên tử khối của nguyên tố và nhờ vào đáp án để xét.
Nguyên tử khối của C = 12
Nguyên tử khối của Ag = 108 = 12 . 9
Nguyên tử khối của C = 40 = 10/3 . 12 = 10/3 nguyên tử khối của C
Câu 6. D
Chỉ cần viết công thức hoá học của những hợp chất theo qui tắc đường chéo, nghĩa là hoá trị của nguyên tố A là chỉ số của nguyên tố B hay nhóm nguyên tử B, và hoá trị của B là chỉ số của A (những chỉ số là số tối giản nhất)
Phần tự luận
a) (3 điểm). Nguyên tử A có (p = 12) có 3 lớp electron lớp 1 có 2 (e), lớp 2 có 8 (e), lớp 3 có 2 (e). Từ đây vẽ sơ đồ cấu trúc nguyên tử cúa A.
b) (2 điểm). Nguyên tử khối của A là: ( dfrac16 2.3 = 24.) đvC
c) (2 điểm). Hạt nhân nguyên tử A có số nơtron là: (24 - 12 =12.)
Loigiaihay.com

Loading Preview
Sorry, preview is currently unavailable. You can tải về the paper by clicking the button above.
 Tải app VietJack. Xem lời giải nhanh hơn!
Tải app VietJack. Xem lời giải nhanh hơn! Xác định thành phần phần trăm những nguyên tố trong 1 mol hợp chất
Bước 1: Tính khối lượng mol của hợp chất.
Bước 2: Tìm số mol nguyên tử mỗi nguyên tố trong 1 mol hợp chất
Ví dụ: Trong 1 mol hợp chất Fe3O4 có: 3 mol nguyên tử Fe, 4 mol nguyên tử O
Bước 3: Tìm thành phần phần trăm những nguyên tố trong hợp chất.
Công thức: %mA =
- Trong số đó:
+ MA là khối lượng mol của A
+ MX là khối lượng mol của hợp chất X
+ a là số mol nguyên tử nguyên tố A có trong 1 mol hợp chất X
Ví dụ 1: Xác định thành phần phần trăm theo khối lượng của những nguyên tố có trong hợp chất KNO3
Hướng dẫn giải:
+ Khối lượng mol của hợp chất: MKNO3 = 39 + 14 + 16.3 = 101 gam/mol
+ Trong 1 mol KNO3 có: 1 mol nguyên tử K; 1 mol nguyên tử N và 3 mol nguyên tử O
+ Thành phần phần trăm theo khối lượng của những nguyên tố là:
%mK = 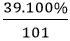
%mN = 
%mO = 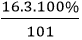
Ví dụ 2: Một hợp chất có công thức hóa học C6H12O6. Hãy cho biết thêm thêm:
a) Khối lượng mol của hợp chất đã cho.
b) Thành phần phần trăm theo khối lượng của những nguyên tố có trong hợp chất.
Hướng dẫn giải:
a) Khối lượng mol của hợp chất:
MC6H12O6 = 12.6 + 1.12 + 16.6 = 180 g/mol
b) Thành phần phần trăm theo khối lượng của những nguyên tố có trong hợp chất:
%mC = 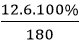
%mH = 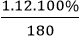
%mO = 100% - (40% + 6,7%) = 53,3%
Ví dụ 3: Cho hai quặng sắt sau: hematit (Fe2O3), manhetit (Fe3O4). Quặng nào chứa hàm lượng sắt cao hơn?
Hướng dẫn giải:
- Hematit (Fe2O3):
+ MFe2O3 = 56.2 + 16.3 = 160 g/mol
+ Trong 1 mol Fe2O3 có: 2 mol nguyên tử Fe
+ %mFe(trong Fe2O3) = 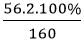
- Manhetit (Fe2O3):
+ MFe3O4 = 56.3 + 16.4 = 232 g/mol
+ Trong 1 mol Fe3O4 có: 3 mol nguyên tử Fe
+ %mFe(trong Fe3O4) = 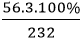
Vậy quặng manhetit (Fe3O4) chứa hàm lượng sắt cao hơn
Câu 1: Cho hợp chất C2H5OH. Số nguyên tử H có trong hợp chất là:
A. 1
B. 5
C. 3
D. 6
Hiển thị đáp án
Đáp án D
Trong hợp chất C2H5OH có 5 + 1 = 6 nguyên tử H
Câu 2: Tính thành phần phần trăm khối lượng của nguyên tố K có trong phân tử K2CO3
A. 56,502%
B. 56,52%
C. 56,3%
D. 56,56%
Hiển thị đáp án
Đáp án B
MK2CO3 = 39.2 +12.1 +16.3 = 138 g/mol
Trong 1 mol K2CO3 có: 2 mol nguyên tử K
%mK = 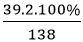
Câu 3: Thành phần phần trăm khối lượng của nguyên tố Na có trong Na3SO4 là:
A. 25%.
B. 32,39%.
C. 31,66%.
D. 38%.
Hiển thị đáp án
Đáp án B
MNa2SO4 = 23.2 +32.1 +16.4 = 142 g/mol
Trong 1 mol Na2SO4 có: 2 mol nguyên tử Na
%mNa = 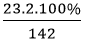
Câu 4: Tính thành phần phần trăm khối lượng nguyên tố Mg có trong 1 mol MgO?
A. 60%
B. 40%
C. 50%
D. 45%
Hiển thị đáp án
Đáp án A
MMgO = 24.1 + 16.1= 40 g/mol
Trong 1 mol MgO có: 1 mol nguyên tử Mg
%mMg = 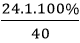
Câu 5: Thành phần phần trăm theo khối lượng của nguyên tố Fe có trong hợp chất Fe2O3 là:
A. 70%
B. 30%
C. 40%
D. 60%
Hiển thị đáp án
Đáp án A
MFe2O3 = 56.2 + 16.3 = 160 g/mol
Trong 1 mol Fe2O3 có: 2 mol nguyên tử Fe
%mFe = 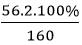
Câu 6: Khối lượng của mỗi nguyên tử Al và O có trong 30,6 gam Al2O3 là:
A. 16 gam và 14,6 gam.
B. 14,4 gam và 16,2 gam.
C. 16,2 gam và 14,4 gam.
D. 14,6 gam và 16 gam.
Hiển thị đáp án
Đáp án C
MAl2O3 = 2.27 + 16.3 = 102 g/mol
Số mol Al2O3 là: nAl2O3 = 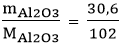
Trong 1 mol Al2O3 có 2 mol nguyên tử Al và 3 mol nguyên tử O
=> trong 0,3 mol Al2O3 có 0,3.2 = 0,6 mol nguyên tử Al và 0,9 mol nguyên tử O
Khối lượng nguyên tử Al là: 0,6.27 = 16,2 gam
Khối lượng nguyên tử O là: 0,9.16 = 14,4 gam
Câu 7: Tính khối lượng Al2O3 biết số mol Al có trong hợp chất là 0,6 mol?
A. 30,6 gam
B. 31 gam
C. 29 gam
D. 11,23 gam
Hiển thị đáp án
Đáp án A
Trong 1 mol Al2O3 có 2 mol nguyên tố Al
Mà số mol Al có trong hợp chất là 0,6 mol → nAl2O3 = 0,3 (mol)
Khối lượng Al2O3 là: mAl2O3 = 0,3.(27.2+16.3) = 30,6 g
Câu 8: Tính khối lượng của Fe trong 92,8 g Fe3O4
A. 67,2 gam
B. 25,6 gam
C. 80 gam
D. 10 gam
Hiển thị đáp án
Đáp án A
MFe3O4 = 56.3 + 16.4 = 232 g/mol
nFe3O4 = 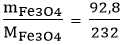
Trong 1 mol Fe3O4 có 3 mol nguyên tử Fe
→ Trong 0,4 mol Fe3O4 có nFe = 3.0,4 = 1,2 mol
Khối lượng của Fe: mFe = 1,2.56 = 67,2 g
Câu 9: Tỉ số về số mol của những nguyên tố C, H, O có trong C3H6O2 là:
A. 3 : 6 : 2
B. 1 : 3 : 1
C. 36 : 6 : 32
D. 12 : 6 : 16
Hiển thị đáp án
Đáp án A
Trong 1 mol C3H6O2 có: 3 mol nguyên tử C, 6 nguyên tử H và 2 nguyên tử O
=> tỉ số về mol của những nguyên tố là: 3 : 6 : 2
Câu 10: Tính tỉ số về khối lượng Một trong những nguyên tố Ca, O, H trong hợp chất Ca(OH)2?
A. 40 : 32 : 3
B. 20 : 16 : 1
C. 10 : 8 : 1
D. 40 : 16 : 2
Hiển thị đáp án
Đáp án B
Trong 1 mol Ca(OH)2 có: 1 mol nguyên tử Ca, 2 nguyên tử O và 2 nguyên tử H
=> khối lượng của Ca là: mCa = nCa . MCa = 1.40 = 40 gam
Khối lượng của O là: mO = nO . MO = 2.16 = 32 gam
Khối lượng của H là: mH = nH .MH = 2.1 = 2 gam
=> tỉ số khối lượng Một trong những nguyên tố là: 40 : 32 : 2 = 20 : 16 : 1
Xem thêm những dạng bài tập Hóa học lớp 8 có đáp án hay khác:
[embed]https://www.youtube.com/watch?v=ieCkGJwl-s8[/embed]
Giới thiệu kênh Youtube VietJack
 Hỏi bài tập trên ứng dụng, thầy cô VietJack trả lời miễn phí!
Hỏi bài tập trên ứng dụng, thầy cô VietJack trả lời miễn phí! - Hơn 20.000 câu trắc nghiệm Toán,Văn, Anh lớp 8 có đáp án
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Nhóm học tập facebook miễn phí cho teen 2k8: fb.com/groups/hoctap2k8/
Theo dõi chúng tôi miễn phí trên social facebook và youtube:Loạt bài Lý thuyết - Bài tập Hóa học lớp 8 có đáp án được biên soạn bám sát nội dung chương trình sgk Hóa học 8.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các phản hồi không phù phù phù hợp với nội quy phản hồi trang web sẽ bị cấm phản hồi vĩnh viễn.
[embed]https://www.youtube.com/watch?v=62vlvKN3VvI[/embed]