Mẹo về Hệ số cân đối của những chất khử trong phản ứng S HNO3 suy ra H2 so4 NO3 là Chi Tiết
Bùi Thị Thu Hương đang tìm kiếm từ khóa Hệ số cân đối của những chất khử trong phản ứng S HNO3 suy ra H2 so4 NO3 là được Update vào lúc : 2022-08-17 09:26:02 . Với phương châm chia sẻ Bí kíp về trong nội dung bài viết một cách Chi Tiết 2022. Nếu sau khi Read nội dung bài viết vẫn ko hiểu thì hoàn toàn có thể lại Comment ở cuối bài để Admin lý giải và hướng dẫn lại nha.
Đáp án B.
Nội dung chính- CÂU HỎI HOT CÙNG CHỦ ĐỀ1. Phản ứng oxi hóa- khử 2. Quy tắc xác định số OXH trong phản ứng OXH - khử.3. Lập phương trình hóa học của phản ứng oxi hóa khử 4. Ý nghĩa của phản ứng oxi hóa tin tức rõ ràng phương trình phản ứng 6HNO3 + S → 2H2O + H2SO4 + 6NO2Điều kiện phản ứng phương trình 6HNO3 + S → 2H2O + H2SO4 + 6NO2 Hiện tượng nhận ra nếu phản ứng xảy ra 6HNO3 + S → 2H2O + H2SO4 + 6NO2 là gì ?tin tức thêm Phương Trình Điều Chế Từ HNO3 Ra H2O Phương Trình Điều Chế Từ HNO3 Ra H2SO4 Phương Trình Điều Chế Từ HNO3 Ra NO2 Phương Trình Điều Chế Từ S Ra H2O Phương Trình Điều Chế Từ S Ra H2SO4 Phương Trình Điều Chế Từ S Ra NO21. Ứng dụng S (sulfua) H2SO4 (axit sulfuric ) NO2 (nitơ dioxit ) tin tức rõ ràng phương trình phản ứng C2H4 + 3O2 → 2H2O + 2CO2Điều kiện phản ứng phương trình C2H4 + 3O2 → 2H2O + 2CO2 Hiện tượng nhận ra nếu phản ứng xảy ra C2H4 + 3O2 → 2H2O + 2CO2 là gì ? Phương Trình Điều Chế Từ C2H4 Ra H2O Phương Trình Điều Chế Từ C2H4 Ra CO2 Phương Trình Điều Chế Từ O2 Ra H2O Phương Trình Điều Chế Từ O2 Ra CO2CO2 (Cacbon dioxit ) tin tức rõ ràng phương trình phản ứng 2O2 + Cu2S → 2CuO + SO2Điều kiện phản ứng phương trình 2O2 + Cu2S → 2CuO + SO2 Hiện tượng nhận ra nếu phản ứng xảy ra 2O2 + Cu2S → 2CuO + SO2 là gì ? Phương Trình Điều Chế Từ O2 Ra CuO Phương Trình Điều Chế Từ O2 Ra SO2 Phương Trình Điều Chế Từ Cu2S Ra CuO Phương Trình Điều Chế Từ Cu2S Ra SO2 Cu2S (Đồng(I) sunfua) SO2 (lưu hùynh dioxit ) tin tức rõ ràng phương trình phản ứng 2H2S + 3O2 → 2H2O + 2SO2Điều kiện phản ứng phương trình 2H2S + 3O2 → 2H2O + 2SO2 Hiện tượng nhận ra nếu phản ứng xảy ra 2H2S + 3O2 → 2H2O + 2SO2 là gì ?tin tức thêm Phương Trình Điều Chế Từ H2S Ra H2O Phương Trình Điều Chế Từ H2S Ra SO2 Phương Trình Điều Chế Từ O2 Ra H2O Phương Trình Điều Chế Từ O2 Ra SO2SO2 (lưu hùynh dioxit ) Hiện tượng nhận ra nếu phản ứng xảy ra 2H2O + O2 + 2SO2 → 2H2SO4 là gì ?
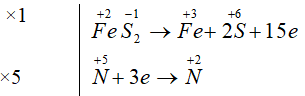
FeS2 + 8HNO3 → Fe(NO3)3 + 2H2SO4 + 5NO + 2H2O
Tổng thông số cân đối của những chất trong phản ứng là = 1 + 8+ 1+ 2+ 5 + 2= 19
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Hãy luôn nhớ cảm ơn và vote 5*
nếu câu vấn đáp hữu ích nhé!

- nhungchu123abc

Đây là một Chuyên Viên, câu vấn đáp của người này mang tính chất chất đúng chuẩn và tin cậy cao
14/12/2022 Cảm ơn 4
Cảm ơn 4XEM GIẢI BÀI TẬP SGK HOÁ 9 - TẠI ĐÂY
 Đặt thắc mắc
Đặt thắc mắc
- lý thuyết trắc nghiệm hỏi đáp bài tập sgk
Lập pt hóa học của những phản ứng oxi hóa - khử sau = pp thăng bằng electron. A) S + HNO3 --> SO2 + NO2 + H2O B) Al + HNO3 --> Al(NO3)3 + N2O + N2 + H2O
Các thắc mắc tương tự
Câu hỏi: Trong phương trình Cu2S + HNO3 -> Cu(NO3)2 + H2SO4 + NO + H2O, thông số của HNO3 là?
A.18
B.22
C.12
D 10
Lời giải:
Đáp án đúng: B. 22
3Cu2S + 22HNO3 -> 6Cu(NO3)2 + 3H2SO4 + 10NO + 8H2O
Cu2S -> Cu2+ + SO42- + 10e
N+5 + 3e -> NO
Cùng Top lời giải tìm hiểu kĩ hơn về cách cân đối phương trình bằng phương pháp thằng bằng electron để hiểu bài tập hơn nhé!
1. Phản ứng oxi hóa- khử
Phản ứng oxi hóa khử là phản ứng hóa học, trong đó có sự chuyển electron Một trong những chất trong phản ứng hay phản ứng oxi hóa khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của một số trong những nguyên tố.
- Chất khử (chất bị oxh) là chất nhường electron
- Quá trình oxh (sự oxh) là quá trình nhường electron.
- Quá trình khử (sự khử) là quá trình thu electron.
Ví dụ: Quá trình thay đổi số oxi hóa:
- Nguyên tử sắt là chất khử. Sự làm tăng số oxi hóa của sắt được gọi là sự việc oxi hóa nguyên tử sắt.
- Nguyên tử sắt nhường electron, là chất khử. Sự nhường electron của nguyên tử sắt được gọi là sự việc oxi hóa nguyên tử sắt.
Cu2+ + 2e → Cu
- Số oxi hóa của đồng giảm từ +2 xuống 0. Ion đồng là chất oxi hóa. Sự làm giảm số oxi hóa của ion đồng được gọi là sự việc khử ion đồng.
- Ion đồng nhận electron, là chất oxi hóa. Sự nhận electron của ion đồng được gọi là sự việc khử ion đồng.
⇒ Phản ứng của sắt với dung dịch đồng sunfat cũng là phản ứng oxi hóa - khử vì tồn tại đồng thời sự oxi hóa và sự khử.
2. Quy tắc xác định số OXH trong phản ứng OXH - khử.
- Số oxi hóa của những nguyên tố trong đơn chất bằng 0.
- Trong hầu hết những hợp chất :
+ Số oxi hóa của H là +1 (trừ những hợp chất của H với sắt kẽm kim loại như NaH, CaH2, thì H có số oxi hóa –1).
+ Số oxi hóa của O là –2 (trừ một số trong những trường hợp như H2O2, F2O, oxi có số oxi hóa lần lượt là : –1, +2).
- Trong một phân tử, tổng đại số số oxi hóa của những nguyên tố bằng 0. Theo quy tắc này, ta hoàn toàn có thể tìm được số oxi hóa của một nguyên tố nào đó trong phân tử nếu biết số oxi hóa của những nguyên tố còn sót lại.
- Trong ion đơn nguyên tử, số oxi hóa của nguyên tử bằng điện tích của ion đó. Trong ion đa nguyên tử, tổng đại số số oxi hóa của những nguyên tử trong ion đó bằng điện tích của nó.
* Chú ý:
- Để màn biểu diễn số oxi hóa thì viết dấu trước, số sau, còn để màn biểu diễn điện tích của ion thì viết số trước, dấu sau. Ví dụ: Số oxi hóa Fe+3 còn ion sắt (III) ghi Fe3+.
- Nếu điện tích là một trong+ (hoặc 1–) hoàn toàn có thể viết đơn giản là + (hoặc -) thì đối với số oxi hóa phải viết đầy đủ cả dấu và chữ (+1 hoặc –1).
3. Lập phương trình hóa học của phản ứng oxi hóa khử
+ Bước 1: Xác định số oxi hóa của những nguyên tố để tìm chất oxi hoá và chất khử.
+ Bước 2: Viết quá trình oxi hóa và quá trình khử, cân đối mỗi quá trình.
+ Bước 3: Tìm thông số thích hợp cho chất oxh và chất khử sao cho tổng số electron cho bằng tổng số electron nhận.
+ Bước 4: Đặt thông số của những chất oxh và khử vào sơ đồ phản ứng, từ đó tính ra thông số những chất khác. Kiểm tra cân đối số nguyên tử của những nguyên tố và cân đối điện tích hai vế để hoàn thành xong PTHH.
* Chú ý: Với phản ứng Oxi hóa khử, cần nhớ:
- Khử cho – O nhận
- Tên của chất và tên quá trình ngược nhau
- Chất khử là chất sẽ nhường electron (hay cho e) - đó quá trình oxi hóa.
- Chất oxi hóa là chất mà thu electron (hay nhận e) - đó là quá trình khử.
4. Ý nghĩa của phản ứng oxi hóa
- Phản ứng oxi hóa - khử là một trong những quá trình quan trọng nhất của thiên nhiên:
- Sự hô hấp, quá trình thực vật hấp thụ khí CO2 giải phóng oxi, sự trao đổi chất và hàng loạt quá trình sinh học khác đều có cơ sở là những phản ứng oxi hóa - khử.
- Ngoài ra: Sự đốt cháy nhiên liệu trong những động cơ, những quá trình điện phân, những phản ứng xảy ra trong pin và trong ăcquy đều gồm có sự oxi hóa và sự khử.
- Hàng loạt quá trình sản xuất như luyện kim, sản xuất hóa chất, chất dẻo, dược phẩm, phân bón hóa học, ... đều không thực hiện được nếu thiếu những phản ứng oxi hóa - khử.
Nếu chưa thấy hết, hãy kéo sang phải để thấy hết phương trình ==>
Xin hãy kéo xuống cuối trang để xem và thực hành những thắc mắc trắc nghiệm liên quan
☟☟☟
tin tức rõ ràng phương trình phản ứng 6HNO3 + S → 2H2O + H2SO4 + 6NO2
6HNO3 + S → 2H2O + H2SO4 + 6NO2 là Phản ứng oxi-hoá khử, HNO3 (axit nitric) phản ứng với S (sulfua) để tạo ra H2O (nước), H2SO4 (axit sulfuric), NO2 (nitơ dioxit) dười điều kiện phản ứng là không còn
Điều kiện phản ứng phương trình 6HNO3 + S → 2H2O + H2SO4 + 6NO2
không còn
Phương Trình Hoá Học Lớp 11 Phản ứng oxi-hoá khử
cho S tác dụng vời dung dịch axit HNO3.
Các bạn hoàn toàn có thể mô tả đơn giản là HNO3 (axit nitric) tác dụng S (sulfua) và tạo ra chất H2O (nước), H2SO4 (axit sulfuric), NO2 (nitơ dioxit) dưới điều kiện nhiệt độ thông thường
Hiện tượng nhận ra nếu phản ứng xảy ra 6HNO3 + S → 2H2O + H2SO4 + 6NO2 là gì ?
Chất rắn màu vàng Lưu huỳnh (S) tan dần và xuất hiện khí nâu đỏ Nito dioxit (NO2) làm sủi bọt khí.
tin tức thêm
Khi đun nóng, HNO3 đặc hoàn toàn có thể oxi hoá được những phi kim như C, S, P
Phương Trình Điều Chế Từ HNO3 Ra H2O
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ HNO3 (axit nitric) ra H2O (nước)
Phương Trình Điều Chế Từ HNO3 Ra H2SO4
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ HNO3 (axit nitric) ra H2SO4 (axit sulfuric)
Phương Trình Điều Chế Từ HNO3 Ra NO2
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ HNO3 (axit nitric) ra NO2 (nitơ dioxit)
Phương Trình Điều Chế Từ S Ra H2O
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ S (sulfua) ra H2O (nước)
Phương Trình Điều Chế Từ S Ra H2SO4
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ S (sulfua) ra H2SO4 (axit sulfuric)
Phương Trình Điều Chế Từ S Ra NO2
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ S (sulfua) ra NO2 (nitơ dioxit)



1. Ứng dụng
Axit nitric là một chất lỏng có màu vàng nhạt đến nâu đỏ, n&oacut ...
S (sulfua)


Lưu huỳnh có nhiều ứng dụng công nghiệp. Thông qua dẫn xuất chính của nó là axít sulfuric (H2SO4), lưu huỳnh được đánh giá là một trong những nguyên tố quan tr� ...



Nước là một hợp chất liên quan trực tiếp và rộng rãi đến sự sống trên Trái Đất, là cơ sở củ ...
H2SO4 (axit sulfuric )



Axit sunfuric là một trong hóa chất rất quan trọng, sản lượng axit sunfuric của một quốc gia hoàn toàn có thể phản ánh về s� ...
NO2 (nitơ dioxit )

.png)

NO2 được sử dụng làm chất trung gian trong sản xuất axit nitric, làm chất nitrat hóa trong sản xuất thuốc nổ hóa học
NO2 cũng khá được ...
Page 2
Nếu chưa thấy hết, hãy kéo sang phải để thấy hết phương trình ==>
Xin hãy kéo xuống cuối trang để xem và thực hành những thắc mắc trắc nghiệm liên quan
☟☟☟
tin tức rõ ràng phương trình phản ứng C2H4 + 3O2 → 2H2O + 2CO2
C2H4 + 3O2 → 2H2O + 2CO2 là Phản ứng oxi-hoá khử, C2H4 (etilen (eten)) phản ứng với O2 (oxi) để tạo ra H2O (nước), CO2 (Cacbon dioxit) dười điều kiện phản ứng là Nhiệt độ: nhiệt độ
Điều kiện phản ứng phương trình C2H4 + 3O2 → 2H2O + 2CO2
Nhiệt độ: nhiệt độ
Phương Trình Hoá Học Lớp 9 Phản ứng oxi-hoá khử
đốt cháy C2H4 trong không khí
Các bạn hoàn toàn có thể mô tả đơn giản là C2H4 (etilen (eten)) tác dụng O2 (oxi) và tạo ra chất H2O (nước), CO2 (Cacbon dioxit) dưới điều kiện nhiệt độ nhiệt độ
Hiện tượng nhận ra nếu phản ứng xảy ra C2H4 + 3O2 → 2H2O + 2CO2 là gì ?
giải phóng khí CO2
Phương Trình Điều Chế Từ C2H4 Ra H2O
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ C2H4 (etilen (eten)) ra H2O (nước)
Phương Trình Điều Chế Từ C2H4 Ra CO2
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ C2H4 (etilen (eten)) ra CO2 (Cacbon dioxit)
Phương Trình Điều Chế Từ O2 Ra H2O
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ O2 (oxi) ra H2O (nước)
Phương Trình Điều Chế Từ O2 Ra CO2
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ O2 (oxi) ra CO2 (Cacbon dioxit)


1. Phản ứng công nghiệp đa phần của ethylene gồm có theo thứ tự quy mô: 1) trùng hợp , 2) quá trình oxy hóa , 3) halogen hóa và hydrohalogenation , 4) alkyl hóa , 5) hydr ...
O2 (oxi)



Oxy là một chất khí không màu, không mùi và không vị là một chất khí thiết yếu cho việc ...



Nước là một hợp chất liên quan trực tiếp và rộng rãi đến sự sống trên Trái Đất, là cơ sở củ ...
CO2 (Cacbon dioxit )



Carbon dioxide được sử dụng trong ngành công nghiệp thực phẩm, công nghiệp dầu mỏ và công nghiệp hóa chất ...
Page 3
Nếu chưa thấy hết, hãy kéo sang phải để thấy hết phương trình ==>
Xin hãy kéo xuống cuối trang để xem và thực hành những thắc mắc trắc nghiệm liên quan
☟☟☟
tin tức rõ ràng phương trình phản ứng 2O2 + Cu2S → 2CuO + SO2
2O2 + Cu2S → 2CuO + SO2 là Phản ứng oxi-hoá khử, O2 (oxi) phản ứng với Cu2S (Đồng(I) sunfua) để tạo ra CuO (Đồng (II) oxit), SO2 (lưu hùynh dioxit) dười điều kiện phản ứng là Nhiệt độ: Nhiệt độ.
Điều kiện phản ứng phương trình 2O2 + Cu2S → 2CuO + SO2
Nhiệt độ: Nhiệt độ.
Phản ứng oxi-hoá khử
cho Cu2S tác dụng với oxi
Các bạn hoàn toàn có thể mô tả đơn giản là O2 (oxi) tác dụng Cu2S (Đồng(I) sunfua) và tạo ra chất CuO (Đồng (II) oxit), SO2 (lưu hùynh dioxit) dưới điều kiện nhiệt độ Nhiệt độ.
Hiện tượng nhận ra nếu phản ứng xảy ra 2O2 + Cu2S → 2CuO + SO2 là gì ?
có khí không màu thoát ra.
Phương Trình Điều Chế Từ O2 Ra CuO
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ O2 (oxi) ra CuO (Đồng (II) oxit)
Phương Trình Điều Chế Từ O2 Ra SO2
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ O2 (oxi) ra SO2 (lưu hùynh dioxit)
Phương Trình Điều Chế Từ Cu2S Ra CuO
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ Cu2S (Đồng(I) sunfua) ra CuO (Đồng (II) oxit)
Phương Trình Điều Chế Từ Cu2S Ra SO2
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ Cu2S (Đồng(I) sunfua) ra SO2 (lưu hùynh dioxit)



Oxy là một chất khí không màu, không mùi và không vị là một chất khí thiết yếu cho việc ...
Cu2S (Đồng(I) sunfua)



Nhìn chung những muối ion hóa hòa tan của đồng độc hại hơn nhiều so với những hợp chất không hòa tan hoặc hơi phân ly. Liều gây chết người của bất kỳ muối � ...


-oxide-unit-cell-3D-balls.png)
Trong thủy tinh, gốm Đồng(II) oxit được dùng trong vật liệu gốm để làm chất tạo sắc tố. Trong môi trường tự nhiên thiên nhiên ôxy hoá thông thường, CuO không biến thành khử thành Cu2O ...
SO2 (lưu hùynh dioxit )



Sản xuất axit sunfuric(Ứng dụng quan trọng nhất) Tẩy trắng giấy, bột giấy, tẩy màu dung dịch đường Đôi khi được dùng làm chất dữ gìn và bảo vệ cho những loại qu ...
Bài học trong sách giáo khoa phương trình có liên quan
Page 4
Nếu chưa thấy hết, hãy kéo sang phải để thấy hết phương trình ==>
Xin hãy kéo xuống cuối trang để xem và thực hành những thắc mắc trắc nghiệm liên quan
☟☟☟
tin tức rõ ràng phương trình phản ứng 2H2S + 3O2 → 2H2O + 2SO2
2H2S + 3O2 → 2H2O + 2SO2 là Phản ứng oxi-hoá khử, H2S (hidro sulfua) phản ứng với O2 (oxi) để tạo ra H2O (nước), SO2 (lưu hùynh dioxit) dười điều kiện phản ứng là Nhiệt độ: 155-250
Điều kiện phản ứng phương trình 2H2S + 3O2 → 2H2O + 2SO2
Nhiệt độ: 155-250
Phương Trình Hoá Học Lớp 10 Phản ứng oxi-hoá khử Phương trình hóa học vô cơ Ôn Thi THPT Quốc Gia 2022
H2S cháy trong không khí cho ngọn lửa màu lam nhạt, khi cho dư oix nó trở thành SO2 và khi thiếu oxi, nó giải phóng lưu huỳnh tự do.
Các bạn hoàn toàn có thể mô tả đơn giản là H2S (hidro sulfua) tác dụng O2 (oxi) và tạo ra chất H2O (nước), SO2 (lưu hùynh dioxit) dưới điều kiện nhiệt độ 155-250
Hiện tượng nhận ra nếu phản ứng xảy ra 2H2S + 3O2 → 2H2O + 2SO2 là gì ?
H2S cháy trong không khí cho ngọn lửa màu lam nhạt,
tin tức thêm
H2S đóng vai trò là chất khử mạnh (S đi từ soxh -2 lên số oxh +4); O2 đóng vai trò là chất oxi hóa (O đi từ số oxh 0 xuống số oxh -2)
Phương Trình Điều Chế Từ H2S Ra H2O
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ H2S (hidro sulfua) ra H2O (nước)
Phương Trình Điều Chế Từ H2S Ra SO2
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ H2S (hidro sulfua) ra SO2 (lưu hùynh dioxit)
Phương Trình Điều Chế Từ O2 Ra H2O
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ O2 (oxi) ra H2O (nước)
Phương Trình Điều Chế Từ O2 Ra SO2
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ O2 (oxi) ra SO2 (lưu hùynh dioxit)



Hydro sunfua được sử dụng đa phần để sản xuất axit sunfuric và lưu huỳnh. Nó cũng khá được sử dụng để tạo ra nhiều loạ ...
O2 (oxi)



Oxy là một chất khí không màu, không mùi và không vị là một chất khí thiết yếu cho việc ...



Nước là một hợp chất liên quan trực tiếp và rộng rãi đến sự sống trên Trái Đất, là cơ sở củ ...
SO2 (lưu hùynh dioxit )



Sản xuất axit sunfuric(Ứng dụng quan trọng nhất) Tẩy trắng giấy, bột giấy, tẩy màu dung dịch đường Đôi khi được dùng làm chất dữ gìn và bảo vệ cho những loại qu ...
Page 5Nếu chưa thấy hết, hãy kéo sang phải để thấy hết phương trình ==>
Xin hãy kéo xuống cuối trang để xem và thực hành những thắc mắc trắc nghiệm liên quan
☟☟☟
2H2O + O2 + 2SO2 → 2H2SO4 là Phản ứng oxi-hoá khử, H2O (nước) phản ứng với O2 (oxi) phản ứng với SO2 (lưu hùynh dioxit) để tạo ra H2SO4 (axit sulfuric) dười điều kiện phản ứng là không còn
Phương Trình Hoá Học Lớp 10 Phản ứng oxi-hoá khử
Không tìm thấy thông tin về cách thực hiện phản ứng của phương trình 2H2O + O2 + 2SO2 → 2H2SO4 Bạn tương hỗ update thông tin giúp chúng mình nhé!
Các bạn hoàn toàn có thể mô tả đơn giản là H2O (nước) tác dụng O2 (oxi) tác dụng SO2 (lưu hùynh dioxit) và tạo ra chất H2SO4 (axit sulfuric) dưới điều kiện nhiệt độ thông thường
Hiện tượng nhận ra nếu phản ứng xảy ra 2H2O + O2 + 2SO2 → 2H2SO4 là gì ?
Phương trình không còn hiện tượng kỳ lạ nhận ra đặc biệt.
Trong trường hợp này, bạn chỉ thường phải quan sát chất sản phẩm H2SO4 (axit sulfuric) (trạng thái: dung dịch) (sắc tố: không màu), được sinh ra
Hoặc bạn phải quan sát chất tham gia H2O (nước) (trạng thái: lỏng) (sắc tố: không màu), O2 (oxi) (trạng thái: khí) (sắc tố: không màu), SO2 (lưu hùynh dioxit) (trạng thái: khí) (sắc tố: không màu), biến mất.
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ H2O (nước) ra H2SO4 (axit sulfuric)
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ O2 (oxi) ra H2SO4 (axit sulfuric)
Trong thực tế, sẽ hoàn toàn có thể nhiều hơn nữa 1 phương pháp điều chế từ SO2 (lưu hùynh dioxit) ra H2SO4 (axit sulfuric)
Nước là một hợp chất liên quan trực tiếp và rộng rãi đến sự sống trên Trái Đất, là cơ sở củ ...
Oxy là một chất khí không màu, không mùi và không vị là một chất khí thiết yếu cho việc ...
Sản xuất axit sunfuric(Ứng dụng quan trọng nhất) Tẩy trắng giấy, bột giấy, tẩy màu dung dịch đường Đôi khi được dùng làm chất dữ gìn và bảo vệ cho những loại qu ...
Axit sunfuric là một trong hóa chất rất quan trọng, sản lượng axit sunfuric của một quốc gia hoàn toàn có thể phản ánh về s� ...
Tải thêm tài liệu liên quan đến nội dung bài viết Hệ số cân đối của những chất khử trong phản ứng S HNO3 suy ra H2 so4 NO3 là
