Mẹo về Cho 1 , 6 gam CuO tác dụng với 100 gam dung dịch h2 so4 20 Mới Nhất
Dương Minh Dũng đang tìm kiếm từ khóa Cho 1 , 6 gam CuO tác dụng với 100 gam dung dịch h2 so4 20 được Cập Nhật vào lúc : 2022-03-28 05:12:05 . Với phương châm chia sẻ Bí quyết Hướng dẫn trong nội dung bài viết một cách Chi Tiết Mới Nhất. Nếu sau khi tham khảo tài liệu vẫn ko hiểu thì hoàn toàn có thể lại Comment ở cuối bài để Ad lý giải và hướng dẫn lại nha.
Bài giải:
1. Phương trình Hoá Học
Phương trình hoá học của phản ứng trên nhờ vào cơ sở phản ứng giữa Oxit bazo yếu với Axit mạnh H2SO4 tạo ra muối mới là CuSO4 có màu xanh và nước.
CuO + H2SO4 → CuSO4 + H2O
[embed]https://www.youtube.com/watch?v=jMkCJl2YYug[/embed]
2. Tính khối lượng axit đã phản ứngChúng ta quan sát theo đề bài ra có số mol của 2 chất tham gia phản ứng đó là của CuO và H2SO4 lần lượt có số mol là 0.085 và
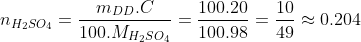
Theo phương trình ra có: CuO + H2SO4 → CuSO4 + H2O Theo PT 1 mol 1 mol Theo bài ra 0.085 0.204 Phản ứng 0.085 0.085 0.085 0.085 Sau phản ứng 0 0.119 0.085 0.085 Vậy số lượng axit đã phản ứng là 0.085 mol và có khối lượng là:
mH2SO4 = 0.085.2+32+64)
mH2SO4 = 8.33 (g)
3. Tính khối lượng muối CuSO4
Sau khi phản ứng thì CuO hết và H2SO4 dư 0.019 mol.
Khối lượng muối sinh ra được tính theo số mol của CuO và có khối lượng của CuSO4 là:
mCuSO4 = 0.085.(64 + 32 + 64)
mCuSO4 = 13.6 (g)
4. Tính nồng độ dung dịch sau phản ứng
Dung dịch sau phản ứng có H2SO4 còn dư và CuSO4 được tạo thành.
Ta có nồng độ % của H2SO4 dư là:
C% H2SO4 =
C% H2SO4 = 10.93 (%)
Nồng độ dung % của CuSO4 là:
C%CuSO4 =
C%CuSO4 = 12.75 (%)
Những tin mới hơn
Những tin cũ hơn

2 trả lời

2 trả lời
n Cu = 1,6 / 80 = 0,02 mol
mH2SO4= (20*100)/100=20g => nH2SO4= 20/98=0.204mol
a)CuO + H2SO4--> CuSO4 + H2O
0.02 0.204 0.204=> Tỉ lệ: 0,02/1 < 0,204/1 => H2SO4 dư ,nH2SO4 dư = 0,204 - 0,02 = 0,182 mol=> m H2SO4 dư = 0,182 . 98 =17,836 g m dd sau p/ư = m dd H2SO4 + m CuO = 100 + 1,6 = 101,6 g => m CuSO4 = 0,02 . 160 = 3,2 g => C% CuSO4 = 3,2 / 101,6 . 100% = 3,15%
=> C% H2SO4dư = 17,836 / 101,6 . 100% = 17,83%
pthh: Cu0+H2so4→cuso4+h2o
n cuo= 1,6: 80=0,02 mol
m h2so4= 20 g→ n h2so4= 0,2 mol
xét tỉ lệ ta thấy : cuo phản ứng hết
n h2so4 dư = 0,2- 0,02= 0,18 mol
m h2so4 dư= 17,64 g
m cuso4 = 0,02. 160=3,2 g
m dd sau p/ ứng= 101,6 g
c %h2so4=17,36%
c %cuso4 = 3,15%
Đáp án:
a) PTHH: CuO + H2SO4 ---> CuSO4 + H2O
b)c% CuSO4 = (mCuSO4 : mdd sau).100% = (3,2 : 101,6).100% = 3,15%
c% H2SO4 dư = (mH2SO4 dư : m dd sau).100% = (18,04:101,6).100% = 17,76%
Giải thích tiến trình giải:
mH2SO4 = mdd H2SO4 . C% :100% = 100.20% : 100% = 20 (g)
=> nH2SO4= mH2SO4 : MH2SO4 = 20 : 98 = 10/49≈ 0,204 (mol)
nCuO = mCuO : MCuO = 1,6:80 = 0,02 (mol)
a) PTHH: CuO + H2SO4 ---> CuSO4 + H2O
Theo pTHH: 1 (mol) 1 (mol)
Theo đề bài: 0,02 (mol) 0,204 (mol)
Ta thấy: 0,02/1 < 0,204/1. Vậy CuO pư hết, H2SO4 dư. Mọi tính toán theo số mol CuO
b) Theo PTHH: nCuSO4 = nCuO = 0,02 (mol) => mCuSO4 = 0,02.160 = 3,2 (g)
nH2SO4 pư = nCuO = 0,02 (mol)
=> mH2SO4 pư = 0,02.98 = 1,96 (g)
=> m H2SO4 dư = mH2SO4 bđ - mH2SO4 dư = 20 - 1,96 = 18,04 (g)
b) Khối lượng dd thu được sau pư là:
mdd sau = mCuO + mdd H2SO4 = 1,6 + 100 = 101,6 (g)
dd sau pư chứa CuSO4 và H2SO4 dư
c% CuSO4 = (mCuSO4 : mdd sau).100% = (3,2 : 101,6).100% = 3,15%
c% H2SO4 dư = (mH2SO4 dư : m dd sau).100% = (18,04:101,6).100% = 17,76%
[embed]https://www.youtube.com/watch?v=2MIRlHjAJy8[/embed]
