Kinh Nghiệm về Bài 2 Thành phần của nguyên tử sách cánh diều Chi Tiết
Hà Huy Tùng Nguyên đang tìm kiếm từ khóa Bài 2 Thành phần của nguyên tử sách cánh diều được Cập Nhật vào lúc : 2022-10-31 23:34:10 . Với phương châm chia sẻ Mẹo Hướng dẫn trong nội dung bài viết một cách Chi Tiết 2022. Nếu sau khi đọc tài liệu vẫn ko hiểu thì hoàn toàn có thể lại phản hồi ở cuối bài để Mình lý giải và hướng dẫn lại nha.Với giải bài tập Hóa 10 Bài 2: Thành phần của nguyên tử sách Cánh diều hay nhất, rõ ràng giúp học viên thuận tiện và đơn giản làm bài tập Hóa học 10 Bài 2.
Giải bài tập Hóa 10 Bài 2: Thành phần của nguyên tử
[embed]https://www.youtube.com/watch?v=C73tMuxYIG0[/embed]
Video giải bài tập Hóa lớp 10 Bài 2: Thành phần của nguyên tử
Mở đầu trang 11 Hóa học 10: Nguyên tử lithium được tạo nên từ ba loại hạt cơ bản (được tô màu rất khác nhau như ở Hình 2.1).Hãy gọi tên và nêu vị trí của mỗi loại hạt này trong nguyên tử.
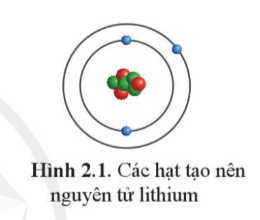
Trả lời:
- Hạt electron màu xanh dương, hạt proton red color, hạt neutron màu xanh lá cây. Như hình minh họa sau:
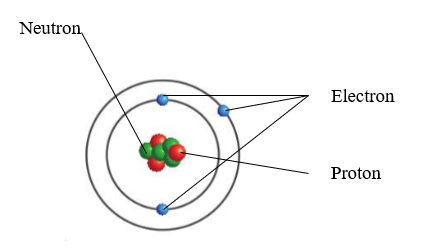 - Vị trí:
- Vị trí:
+ Hạt electron ở vỏ nguyên tử;
+ Hạt proton và neutron ở hạt nhân nguyên tử.
I. Thành phần và cấu trúc của nguyên tử
1. Thành phần nguyên tử
Câu hỏi1 trang 11 Hóa học 10: Các nguyên tử đều trung hòa về điện. Dựa vào bảng 2.1, em hãy lập luận để chứng tỏ rằng: Trong một nguyên tử, số proton và số electron luôn bằng nhau.

Trả lời:
Giả sử trong một nguyên tử bất kì:
- Có x hạt proton, mỗi hạt proton có điện tích +1.
⇒ Tổng số điện tích dương là +x
- Có y hạt electron, mỗi hạt electron có điện tích -1
⇒ Tổng số điện tích âm là –y.
Nguyên tử trung hòa về điện nên: tổng số điện tích dương + tổng số điện tích âm = 0
⇒ (+x) + (-y) = 0 ⇔ x = y
Vậy trong một nguyên tử bất kì số proton và số electron luôn bằng nhau.
Luyện tập 1 trang 12 Hóa học 10: Hạt proton, neutron nặng hơn hạt electron bao nhiêu lần?
Trả lời:
Khối lượng hạt proton ≈ khối lượng hạt neutron ≈ 1 amu
Khối lượng hạt electron ≈ 0,00055 amu
⇒ Hạt proton, neutron nặng hơn hạt electron là 10,00055 ≈ 1818 lần
Luyện tập 2 trang 12 Hóa học 10: Hãy cho biết thêm thêm bao nhiêu hạt proton thì có tổng khối lượng bằng 1 gam.
Trả lời:
1 amu = 1,6605.10-27kg= 1,6605.10-24 g
1 hạt proton có khối lượng ≈ 1,6605.10-24 gam
x hạt proton có khối lượng = 1 gam
⇒ x ≈ 11,6605.10−24 = 6,022.1023 hạt
2. Cấu trúc của nguyên tử
Luyện tập 3 trang 12 Hóa học 10:Khi những nguyên tử tiến lại gần nhau để hình thành link hóa học, sự tiếp xúc đầu tiên giữa hai nguyên tử sẽ xảy ra giữa
A. lớp vỏ với lớp vỏ.
B. lớp vỏ với hạt nhân.
C. hạt nhân với hạt nhân.
Trả lời
Đáp án đúng là: A
Khi những nguyên tử tiến lại gần nhau để hình thành link hóa học, sự tiếp xúc đầu tiên giữa hai nguyên tử sẽ xảy ra giữa lớp vỏ với lớp vỏ.
Câu hỏi2 trang 12 Hóa học 10: Hãy chỉ ra những sự rất khác nhau về thành phần nguyên tử giữa nguyên tử hydrogen và beryllium được minh họa trong Hình 2.2
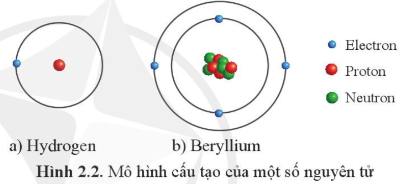
Trả lời:
Nguyên tử beryllium có neutron trong hạt nhân còn nguyên tử hydrogen không còn neutron trong hạt nhân.
II. Khối lượng và kích thước của nguyên tử
1. Khối lượng của nguyên tử
Luyện tập 4 trang 12 Hóa học 10:Nguyên tử lithium (Li) tạo nên là 3proton, 4 neutron và 3electron. Khối lượng lớp vỏ của Li bằng khoảng chừng bao nhiêu phần trăm khối lượng của tất cả nguyên tử Li?
Trả lời:
Nguyên tử lithium (Li) tạo nên là 3p, 4n và 3e nên khối lượng của một nguyên tử Li là:
3.1 + 4.1 + 3.0,00055 = 7,00165 (amu)
Khối lượng lớp vỏ của Li là: 3.0,00055 = 1,65.10-3 amu.
Phần trăm khối lượng lớp vỏ: 1,65.10 −37,00165.100%=0,024%.
2. Kích thước của nguyên tử
Luyện tập 5 trang 13 Hóa học 10:Hồng cầu được coi như có dạng đĩa tròn với đường kính 7,8 ×104Ao . Hỏi cần bao nhiêu nguyên tử Fr sắp xếp thẳng hàng và khít nhau để tạo nên một đoạn thẳng có chiều dài bằng đường kính của hồng cầu?
Trả lời:
Một nguyên tử Fr có đường kính bằng 7,0Ao
Cần số nguyên tử Fr là: 7,8×1047,0 ≈ 11143 nguyên tử
Vận dụng trang 13 Hóa học 10: J.J. Thomson (J.J. Tôm – xơn), nhà vật lí người Anh, được trao phần thưởng Nobel (Nô-ben)Vật lí vào năm 1906 vì đã phát hiện ra một loại hạt cơ bản tạo nên nguyên tử. Thomson đã sản xuất ống tia âm cực gồm một ống thủy tinh được hút phần lớn không khí ra khỏi ống, một hiệu điện thế cao được đặt vào hai điện cực gắn ở hai đầu ống (Hình 2.4a). Năm 1897, ông phát hiện ra một dòng hạt (tia) đi ra từ điện cực tích điện âm (cực âm) sang điện cực tích điện dương (cực dương). Tia này được gọi là tia âm cực.
Các loại hạt tạo nên tia âm cực có đặc điểm: (1) Chuyển động theo đường thẳng trong ống (Hình 2.4a). (2) Hoàn toàn giống nhau dù những vật liệu làm cực âm rất khác nhau. (3) Bị lệch trong điện trường, về phía bản cực tích điện dương được đặt giữa ống tia âm cực (Hình 2.4b).
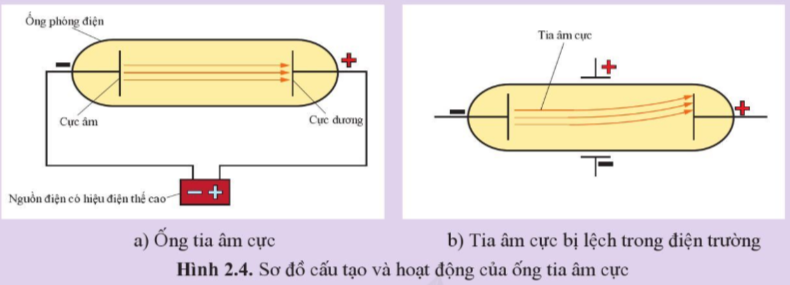
Hãy cho biết thêm thêm hạt tạo nên tia âm cực là loại hạt gì. Giải thích.
Trả lời:
Dựa trên những đặc điểm về tia âm cực xác định được: Hạt tạo nên tia âm cực là hạt electron vì electron mang điện tích âm nên sẽ bị lệch trong điện trường, về phía bản cực tích điện dương.
Bài tập (trang 15)
Bài 1 trang 15 Hóa học 10: Một loại nguyên tử hydrogen có cấu trúc đơn giản nhất, được tạo nên chỉ có thể từ 1 electron và 1 proton. Những phát biểu nào sau đây là đúng khi nói về nguyên tử hydrogen này?
(a) Đây là nguyên tử nhẹ nhất trong số những nguyên tử được biết cho tới nay.
(b) Khối lượng nguyên tử xấp xỉ 2 amu.
(c) Hạt nhân nguyên tử có khối lượng gấp khoảng chừng 1818 lần khối lượng lớp vỏ.
(d) Kích thước của nguyên tử bằng kích thước của hạt nhân.
Trả lời:
(a) Đúng. Khối lượng nguyên tử xấp xỉ 1 amu. Là nguyên tử nhẹ nhất trong số những nguyên tử được biết cho tới nay.
(b) Sai. Khối lượng nguyên tử xấp xỉ 1 amu.
(c) Đúng. Khối lượng hạt proton ≈ 1 amu
Khối lượng hạt electron ≈ 0,00055 amu
⇒ Khối lượng hạt nhân nguyên tử to hơn khối lượng lớp vỏ là 10,00055 ≈ 1818 lần
(d) Sai. Kích thước của hạt nhân rất nhỏ so với kích thước của nguyên tử.
Bài 2 trang 15 Hóa học 10: Các đám mây gây hiện tượng kỳ lạ sấm sét tạo nên là những hạt nước nhỏ li ti mang điện tích. Một phép đo thực nghiệm đã cho tất cả chúng ta biết một giọt nước có đường kính 50 μm, mang một lượng điện tích âm là -3,33 × 10-17C. Hãy cho biết thêm thêm điện tích âm của giọt nước trên tương đương với điện tích của bao nhiêu electron.
Trả lời:
Điện tích của một hạt electron là -e0 = -1,602 × 10-19C
Điện tích âm của giọt nước trên tương đương với điện tích của số electron là:
−3,33 × 10−17−1,602 × 10−19 ≈ 208 electron
Bài 3 trang 15 Hóa học 10: Nguyên tử trung hòa về điện vì
A. được tạo nên là những hạt không mang điện.
B. có tổng số hạt proton bằng tổng số hạt electron.
C. có tổng số hạt electron bằng tổng số hạt neutron.
D. tổng số hạt neutron bằng tổng số hạt proton.
Trả lời:
Nguyên tửtrung hòa về điện vì có tổng số hạt proton bằng tổng số hạt electron.
Bài 4 trang 15 Hóa học 10: Trả lời những thắc mắc sau:
a) Loại hạt nào được tìm thấy trong hạt nhân nguyên tử?
b) Loại hạt nào được tìm thấy ở lớp vỏ nguyên tử?
c) Loại hạt nào mang điện trong nguyên tử?
d) Kích thước nguyên tử to hơn kích thước hạt nhân nguyên tử khoảng chừng bao nhiêu lần?
Trả lời:
a) Loại hạt được tìm thấy trong hạt nhân nguyên tử là:
+ Hạt proton (kí hiệu là p),
+ Hạt neutron (kí hiệu là n).
b) Loại hạt được tìm thấy ở lớp vỏ nguyên tử là:
+ Hạt electron (kí hiệu là e)
c) Loại hạt mang điện trong nguyên tử là:
+ Hạt proton, mang điện tích dương.
+ Hạt electron, mang điện tích âm.
d) Kích thước nguyên tử to hơn kích thước hạt nhân nguyên tử khoảng chừng 104 đến 105 lần.
Bài 5 trang 15 Hóa học 10: Tính tổng số electron, proton và neutron trong một phân tử nước (H2O). Biết trong phân tử này, nguyên tử H chỉ gồm 1 proton và 1 electron; nguyên tử O có 8 neutron và 8 proton.
Trả lời:
Chú ý: Trong nguyên tử số electron = số proton
Số electron
Số proton
Số neutron
H
1
1
0
O
8
8
8
H2O
1 × 2 + 8 = 10
1 × 2 + 8 = 10
8
Xem thêm lời giải bài tập Hóa học lớp 10 Cánh diều hay, rõ ràng khác:
Bài 3: Nguyên tố hóa học
Bài 4: Mô hình nguyên tử và orbital nguyên tử
Bài 5: Lớp, phân lớp và thông số kỹ thuật electron
Bài 6: Cấu tạo của bảng tuần hoàn những nguyên tố hóa học
Bài 7: Xu hướng biến hóa một số trong những tính chất của đơn chất, biến hóa thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm
Xem thêm tài liệu Hóa học lớp 10 Cánh diều hay, rõ ràng khác:
Lý thuyết Bài 2: Các thành phần của nguyên tử
Trắc nghiệm Bài 2. Thành phần của nguyên tử
Tải thêm tài liệu liên quan đến nội dung bài viết Bài 2 Thành phần của nguyên tử sách cánh diều